Литий
Революцию в технике, нацеленной на потребительские рынки, произвели легкие литий-ионные аккумуляторы.

- плотность примерно соответствует сосновой древесине (в 2 раза меньше, чем у воды, и может в ней плавать):
- мягкий, серебристо-белый щелочной металл;
- не встречается в природе в виде металла, но встречается в сочетании в небольших количествах почти во всех магматических породах и в водах многих минеральных источников;
- наиболее важными минералами, содержащими литий, являются сподумен, петалит, лепидолит и амблигонит;
- необходимо хранить в вакууме, инертной атмосфере или в инертной жидкости, такой как очищенный керосин или минеральное масло, поскольку он, как и все щелочные металлы, обладает высокой реакционной способностью и воспламеняемостью.
Применение
Первым применением лития (в качестве добавки) стало производство высокотемпературных смазок, вторым – высокопрочные термостойкие стекло и керамика (в том числе противоударная посуда).
Но настоящую революцию в технике, нацеленной на потребительские рынки, произвели легкие литий-ионные аккумуляторы.
При равном весе они производят больше энергии, чем все другие подобные источники питания или, проще говоря, имеют более высокую плотность энергии.
Такие аккумуляторы используются в смартфонах, ноутбуках, электромобилях, БПЛА, электроинструментах, роботах и прочей технике.
Литий также используется в некоторых неперезаряжаемых батареях для такой продукции, как кардиостимуляторы, игрушки и часы.
Металлический литий получают в виде сплавов с алюминием и магнием, повышающих их прочность и делающих их легче.
Магниево-литиевый сплав используется для покрытия брони.
Алюминиево-литиевые сплавы используются в самолетах, велосипедных рамах и высокоскоростных поездах.
Оксид лития используется в специальных стеклах и стеклокерамике.
Хлорид лития является одним из наиболее гигроскопичных известных материалов и используется в системах кондиционирования воздуха и промышленной сушки (как и бромид лития).
Стеарат лития используется в качестве универсальной смазки при высоких температурах.
Карбонат лития используется в лекарствах для лечения маниакально-депрессивного состояния, хотя его действие на мозг до сих пор до конца не изучено.
Гидрид лития используется в качестве средства хранения водорода для использования в качестве топлива.
На сегодня порядка 3/4 лития потребляет аккумуляторная промышленность.
Водород для водородных бомб
Для любознательных напомним, что водород для водородных бомб на самом деле представляет собой сложный гидрид лития, в котором литий является изотопом лития-6, а водород — изотопом водорода-2 (дейтерий).
Это соединение способно выделять огромное количество энергии из нейтронов, выпущенных атомной бомбой в ее ядре.
Они поглощаются ядрами лития-6, который немедленно распадается с образованием гелия и водорода-3, которые затем переходят в другие элементы.
При этом бомба взрывается с силой в миллионы тонн тротила.
Добыча
Литий — очень активный химически металл, поэтому его добыча ведется несколько отличными от добычи большинства прочих, обычных металлов способами.
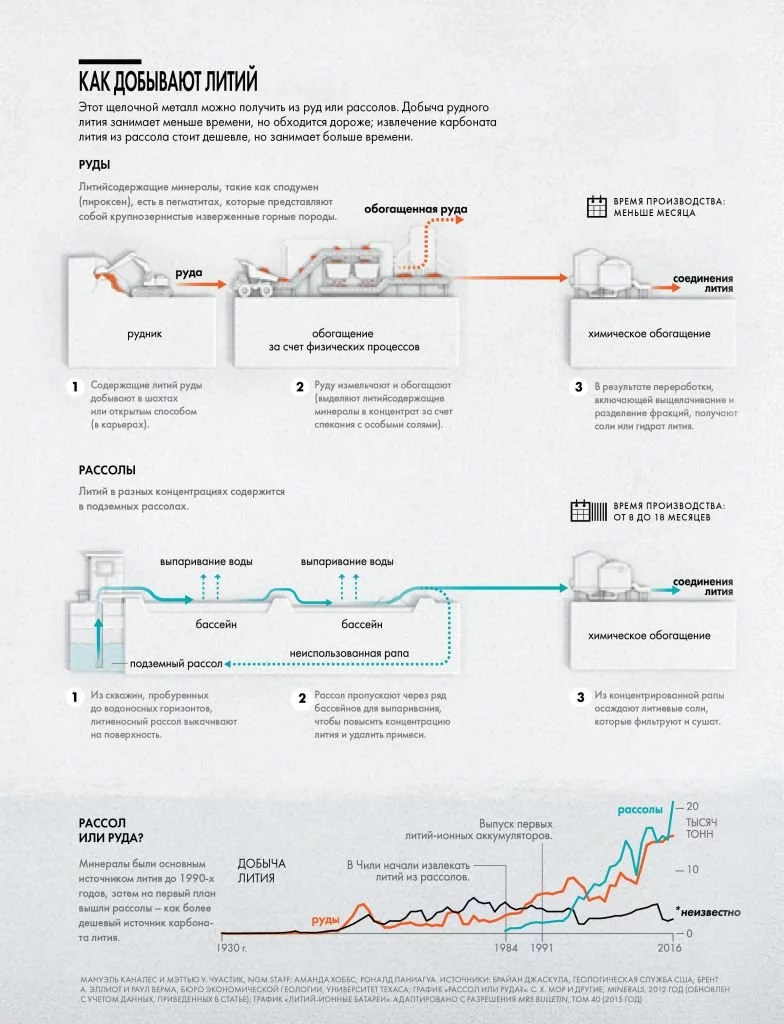
Мировое потребление лития в 2021 г. выросло на 33% по сравнению с 2020 г. (с 70 до 93 тыс. т) что не замедлило сказаться на увеличении предложения.
Это самый быстрорастущий рынок какого-либо металла.
В 2021 г. наибольшее количество лития было добыто в Австралии (55 тыс. т), Чили (26 тыс. т) и Китае (14 тыс. т).
Однако этот список может существенно поменяться — Боливия и ДРК вплотную подошли к масштабной коммерческой разработке.
В Чили большая часть лития производится из рассолов, которые при обработке карбонатом натрия дают карбонат лития.
Металл получают электролизом расплавленного хлорида лития и хлорида калия.
- выпариванием воды из соляных рассолов и переработкой оставшихся твердых веществ (хлорида натрия, хлорида калия и хлорида лития);
- добычей из твердых горных пород;
- фильтрацией веществ, выносимых на поверхность в геотермальных скважинах.
Мировые запасы
Литий довольно распространен, однако нигде и никогда не встречается в чистом в виде из-за своей высокой реакционной способности (приходиться выделять методом электролиза).
Его содержание в горной породе и рассолах сильно варьируется, а потому коммерческое извлечение не везде оправдано.
В Мировом океане содержится 230 млрд т лития, однако в крайне низкой концентрации.
При существующих технологиях его добыча из морской воды не имеет экономического смысла.
РФ
В России самые большие потенциальные запасы лития находятся в Мурманской области.
Также есть залежи в Дагестане и Якутии.
Самое перспективное месторождение Дагестана, по оптимистичным прогнозам, способно давать до 6 тыс. т/год.
Однако сообщений о том, что российские запасы лития начали разрабатываться, до настоящего времени не было.
Литий (Li)

Литий — первый щелочной металл в периодической таблице элементов. В природе он находится в смешанной форме изотопов Li 6 и Li 7. Литий — самый легкий металл, он мягкий, с низкой температурой плавления. Многие из его физических и химических свойств больше похожи на свойства щелочноземельных металлов, чем на свойства его собственной группы. Доля лития в земной коре составляет 65 частей на миллион.
Свойства
Среди наиболее важных свойств лития — высокая удельная теплоемкость, высокая теплопроводность, низкая вязкость и очень низкая плотность. Металлический литий растворим в коротких олефатических полиаминах и этиламине, не растворяется в углеводородах.
Литий вступает в большое количество реакций с органическими реагентами, а также с неорганическими реагентами. Реагирует с кислородом с образованием моноксида и гипероксида. Это единственный щелочной металл, который реагирует с азотом при температуре окружающей среды с образованием черной азотной кислоты. Он бурно реагирует с водой и легко реагирует с водородом при температуре почти 500 C с образованием гидрида лития. Реагирует с углеродом с образованием карбонидов.
Легко связывается с галогенами, образуя галогениды с яркими спектральными линиями излучения. Хотя он не реагирует с парафиновыми углеводородами, он реагирует с алкенами в реакциях присоединения, заменяя двойные связи и диеновые группы. Он также вступает в реакцию с соединениями ацетилена и образует ацетилен лития, который играет важную роль в синтезе витамина А.
Литий взрывоопасен: опасность пожара и взрыва возникает при контакте с горючими веществами и водой. Вдыхание газов лития может привести к появлению симптомов жжения, раздражения, кашля, затрудненного дыхания и воспаления гортани. Симптомы отека легких часто не очевидны и становятся заметными только через несколько часов из-за физической слабости.
Применение
Литий — самый легкий из всех элементов и поэтому используется во многих областях. Например, для сплавов с алюминием и магнием, а также со свинцом, чтобы сделать их более стабильными и в то же время более легкими. Одним из наиболее важных применений является использование лития для батарей и аккумуляторов.
В качестве флюса в стекольной промышленности и в качестве добавки к глазури карбонат лития снижает вязкость веществ и облегчает их обработку. Другие соединения лития используются в качестве загустителей жиров и масел.
Хлорид лития — одно из твердых веществ, обладающих самой высокой способностью абсорбировать воду. Поэтому его используют в системах кондиционирования воздуха и для осушения промышленных газов. Соединения лития также подходят в качестве антифриза.
Некоторые соединения лития хорошо подходят в качестве смазочных материалов, поскольку их можно использовать как при очень высоких, так и при очень низких температурах. Литий показал хорошие результаты в лечении маниакально-депрессивных пациентов. В форме гидроксида лития (LiOH) он используется в качестве очистителя воздуха с сильным связыванием CO2.
Воздействие лития на здоровье
Содержание лития в организме человека составляет около 7 мг. Биологическая польза лития неизвестна, поэтому только небольшая его часть усваивается организмом, а излишки быстро выводятся. Карбонат лития используется в психиатрических целях в дозах, близких к пределу токсичности. При количестве 10 мг / л крови говорят о легком отравлении литием, 15 мг / л способствуют таким эффектам, как спутанность сознания и невнятная речь, а при концентрации около 20 мг / л существует угроза смерти.
Контакт с кожей может вызвать покраснение, раздражение и волдыри. Пероральный прием лития может вызвать спазмы в животе, что может привести к жгучей боли, тошноте, рвоте, чувству слабости или даже коме.
Воздействие лития на окружающую среду
Металлический литий реагирует с азотом, кислородом и водяным паром в присутствии воздуха. На поверхности лития образуется оксидный слой, в результате чего образуется гидроксид (LiOH), карбонат лития (Li2CO3) и нитрид лития (Li3N). Гидроксид лития представляет собой потенциальную опасность, поскольку он чрезвычайно агрессивен.
Опасность химического воздействия: сильный нагрев лития может вызвать сильный пожар или взрыв. Вещество может самовоспламеняться при контакте с воздухом, если оно мелко измельчено. При нагревании образуются токсичные пары. Литий бурно реагирует с сильными окислителями, кислотами и многими соединениями (углеводороды, галогены, бетон, песок и асбест). При реакции с водой образуются газообразный водород и коррозионные пары гидроксида лития, которые легко воспламеняются.
Литий и вода
Минеральная вода содержит 0,05–1 мг лития на литр. Литий также был обнаружен в больших количествах в лечебных водах Карлсбада, Мариенбада и Виши. В растворенном виде он встречается исключительно как Li + (водн.).
Как и в каких соединениях литий реагирует с водой?
Литий бурно реагирует с водой, образуя гидроксид лития и выделяя чрезвычайно легковоспламеняющийся водород. Однако экзотермическая реакция протекает медленнее, чем реакция натрия с водой, которая находится непосредственно под литием в периодической таблице.
При 750 C литий реагирует с водородом с образованием гидрида лития LiH. В результате получается белый порошок, который в более поздней реакции с водой выделяет газообразный водород, а именно 2800 литров на килограмм гидрида.
Растворимость лития и / или его соединений в воде
Литий в своей элементарной форме не растворяется в воде, но реагирует с ней. С другой стороны, соединения лития, такие как хлорид лития, карбонат лития, фосфат лития, фторид лития и гидроксид лития, могут быть более или менее растворимыми в воде. Последнее соединение имеет, например, растворимость в воде 129 г / л.
Как литий может попасть в воду?
Литий содержится во многих минералах, но прежде всего в амблигоните, петалите, лепидолите и сподумене. Для коммерческих целей лучше всего подходит сподумен (LiAl Si2O6).
Литий, относящийся к 1 классу опасности для воды (незначительно опасен), не представляет серьезной угрозы для растений и животных ни на суше, ни в водных экосистемах. Литий не считается необходимым элементом для роста растений. Слишком большое содержание лития может быть даже токсично для некоторых видов. Этому можно противодействовать, добавляя известь в почву, поскольку кальций препятствует усвоению более легких минералов. Содержание лития в различных растениях обычно составляет от 0,2 до 30 частей на миллион.
Источник https://neftegaz.ru/tech-library/materialy/785470-litiy/
Источник https://snab365.ru/lithium/